Использование сегментации коры и индивидуальных 3д печатных краниометрических линеек для удаления конвекситальных образований мозга
Открытые микрохирургические операции на конвекситальных отделах коры головного мозга выполняются часто. Для успешного их выполнения требуется хорошее ориентирование в индивидуальной (для данного пациента) конвекситальной анатомии. Качественное выполнение таких операций подразумевает так же использование минимальной, но достаточной краниотомии. Обычно для обеспечения этих двух ключевых моментов используется безрамная нейронавигация [1]. Однако навигационные системы могут не обеспечивать необходимой точности если пользователи совершают ошибки при регистрации пациента и интерпретации данных [2]. Процесс настройки навигатора занимает часть операционного времени (≈ 30 минут), увеличивая продолжительность вмешательства. Следует так же указать на высокую цену качественных современных систем навигации.
В настоящее время печать хирургических шаблонов стала проста и доступна, но преимущественно используется стоматологами [4 - 6]. 3D-печатные шаблоны так же активно используются ортопедами-травматологами [7, 8]. Опубликован ряд работ об использовании печатных хирургических шаблонов для установки транспедикулярных винтов [9 - 11]. Накладные на скальп хирургические шаблоны использованы рядом авторов для стереотаксической пункции гематом [12, 13]. Однако мы не нашли ни одной публикации по использованию хирургических шаблонов для разметки при нейрохирургических операциях. Возможно потому что моделирование и печать представляется врачам достаточно сложными, мы, однако, считаем, что при наличии достаточно базовых навыков моделирования и печати, методика проста и масштабируема [14]. В данной работе мы предлагаем способ навигации для хирургии конвекситальных образований головного мозга, отличающийся высокой точностью и низкой ценой.
Описание метода
Способ заключается в использовании двух элементов: сегментации (создания модели индивидуальной анатомии) коры головного мозга в области интереса и печати индивидуальной краниометрической линейки. В приведенном примере сегментация выполнена по T1-взвешенной 3d МРТ последовательности без контраста с помощью Inobitec DICOM viewer 2.6. Моделирование краниометрической линейки выполнялось в Blender 2.93.
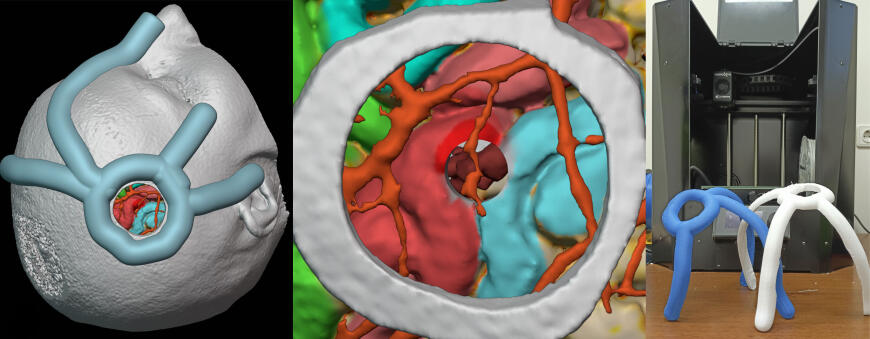
Краниометрические линейки моделировались по сегментированной поверхности головы и представляли собой фигуры, срезанные поверхностью кожи. Типичная линейка состояла из кольца, описывающего проекцию краниотомии на кожу, и трех лучей, тянущихся в большинстве случаев к трем опорным неровностям: у правого и левого козелков и на переносицу. Как показал наш опыт, использование трех названных опорных точек и большая площадь соприкосновения с поверхностью головы обеспечивают точное позиционирование линейки, не уступающее правильной разметке с использованием навигатора.
Для печати обычно использовались два fdm/fff принтера Picaso Designer X Pro (сопло 0.5 мм) и Geralkom Prusa i3 Steel (сопло 0.6 мм). Нарезка выполнялась в слайсерах Polygon X 2.3.0 и Ultimaker Cura 4.62. Обычные параметры печати: высота слоя 0.3 - 0.4, ширина линии 0.65 - 0.75, количество стенок - 2, скорость периметров - 60 - 80 мм/сек. Печать производилась материалами PETg или PLA и занимала обычно от 2 до 4 часов. Краниометрическая линейка считалась верифицированной при полном соответствии поверхности головы пациента. Вариант моделирования линеек приведен далее на видео.
Клинические данные
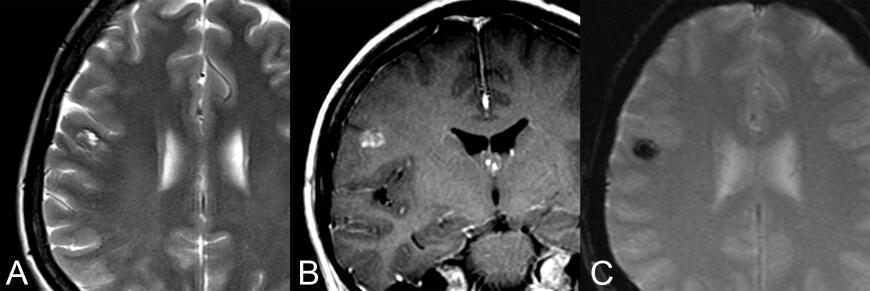
Пациент обследован по поводу двух фокальных приступов в лице и руке. При МРТ выявлена небольшая кавернома латеральных отделов правой предцентральной извилины (рис. 1). В связи с очевидной связью между симптоматикой и наличием каверномы решено выполнить ее удаление. Кавернома имела достаточно малые размеры и была расположена в функционально значимой области (моторная кора), в связи с чем для ее успешного удаления необходимо было использовать одну из методик навигации.
Рис 1. Кавернома латеральных отделов правой прецентральной извилины на МРТ в разных режимах: A – T2, B – T1+Gd, C – T2*GRE
Подготовка к операции
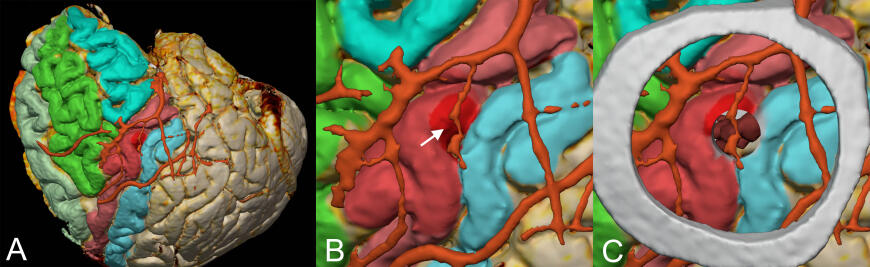
Кора головного мозга и кавернома сегментированы по данным МРТ. Согласно общеизвестным анатомическим представлениям цветом выделены извилины: лобные, прецентральная, постцентральная (рис. 2). Выбран доступ, заключающийся в диссекции латеральных отделов роландовой борозды и энцефалотомии в области ее дна, что обеспечит минимальную травматизацию окружающих структур. Так же по Т1 с контрастом сегментированы оболочечные артерии.
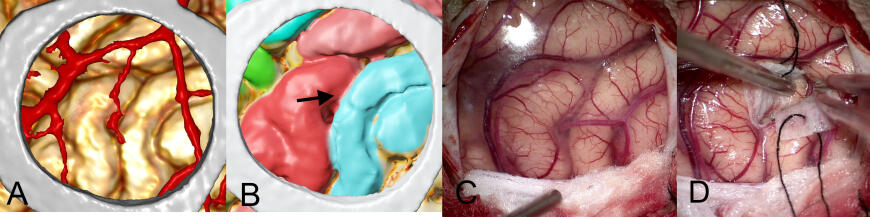
Рис 2. А – общий вид конвекситальной коры справа с цветовым обозначением извилин: лобных, предцентральной и постцентральной. B - область вмешательства, стрелкой указана проекция каверномы на поверхность прецентральной извилины, С – запланированный размер трепанации обозначен с помощью контура, выделенного из поверхности головы по МРТ, по ходу предполагаемого доступа из модели коры удален небольшой цилиндр, что позволяет визуализировать каверному.
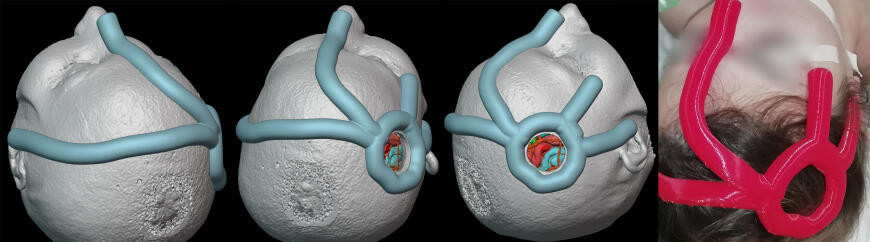
Для максимально точной разметки перед краниотомией смоделирована в Blender 2.93 и напечатана из PETg. Созданная модель состояла из кольца, внутренняя часть которого описывала проекцию необходимой краниотомии, и четырех лучей ориентированных на 4 точки: область переносицы, правый и левый козелки, правый наружный угол глаза (рис. 3).
Рис. 3. Разметка области операции с помощью индивидуальной краниометрической линейки.
Операция
Из линейного разреза кожи согласно разметке выполнена краниотомия. На поверхности оболочки выявлены менингеальные артерии, соответствующие сегментированным. Вскрыта твердая мозговая оболочка. Выявлено соответствие между структурами обнаженной коры и сегментированной моделью (рис.4), четко идентифицирована прецентральная извилина и область запланированной диссекции в латеральных отделах центральной борозды. Оценены моторные вызванные потенциалы, выявлено представительство лица в этой области, тем не менее наиболее безопасным признан запланированный ранее доступ. Диссекция борозды и энцефалотомия в глубине борозды, на небольшой глубине выявлена кавернома. Образование удалено без резекции перифокальных отложений гемосидерина. В послеоперационном периоде нарастания фокального неврологического дефицита не отмечалось, однако были жалобы на фокальные судороги в области верхней губы слева в связи с чем назначены антиконвульсанты.
Рис. 4. A – сегментированные по МРТ оболочечные артерии , B - сегментированный рисунок коры соответствует интраоперационному (C), D– диссекция латеральных отделов центральной борозды, на небольшой глубине выявлена кавернома
Обсуждение
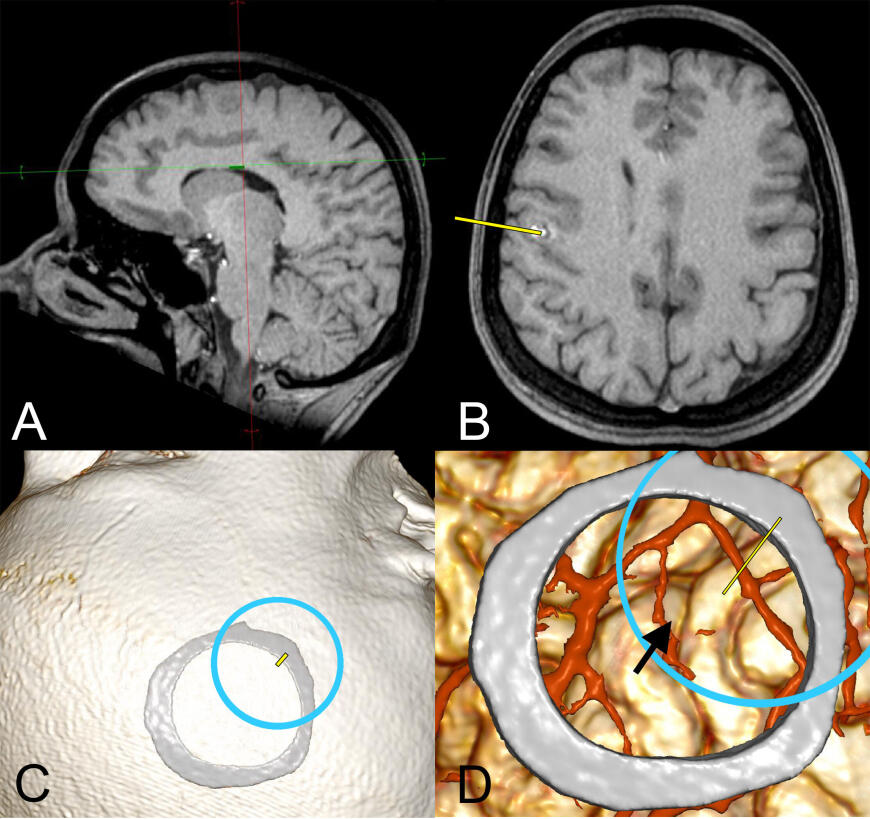
Интраоперационное использование нейронавигации безусловно оказывает существенную помощь хирургу [1]. Однако, при использовании нейронавигации существует ряд моментов, на которые необходимо указать [2]. Как и с любым другим инструментом, с нейронавигатором надо уметь работать. Необходимый и очень важный этап при использовании этих систем – регистрация пациента, представляющая собой синхронизацию между загруженными в нейронавигатор снимками и положением головы на операционном столе. Данный процесс в зависимости от опыта пользователя может увеличивать общее операционное время на 10-30 минут [3]. Ошибки в регистрации пациента совершаются достаточно часто. Порой расхождение в координатах ± 1 сантиметр воспринимается как допустимое, но в случае поиска небольших образований такая ошибка будет значимой. В процессе манипуляций с пациентом положение якорных точек по отношению к пациенту может быть нарушено. Такое возможно, например, при изменении положения головы в фиксирующем устройстве [15]. В процессе операции при замене нестерильных инструментов на стерильные могут возникать расхождения в случае если геометрия инструментов нарушена [16]. Следует отметить высокую цену хороших современных безрамных нейронавигаторов и необходимость их регулярного обслуживания специалистом, что иногда игнорируется. Для некоторых локализаций, при использовании снимков с нестандартным (чаще переразогнутым) положением головы без коррекции угла гентри у неопытных пользователей могут возникать ошибки при разметке доступа [17]. Расстояние между поверхностью кожи и поверхностью мозга обычно невелико, однако, при планировании мини краниотомии и наличии значимого угла наклона в используемой серии, пользователь находит и отмечает смещенную проекцию образования на поверхность, при этом смещая весь доступ (рис. 5.). Чтобы подобного не происходило необходимо ориентироваться минимум по двум проекциям, и желательно использовать встроенные возможности навигатора по сегментации и в 3d представлении данных. Так же необходимо понимать, то в навигатор загружены данные по состоянию на момент исследования, а в процессе операции вследствие дренирования ликвора, удаления и тракции вещества, положение структур может значимо меняться [15].
Рисунок 5. Смоделирована частая ошибка при разметке доступа с помощью навигации. A –голова переразогнута, зеленая линия параллельна сечениям аксиальной проекции. B – центр доступа намечен только по аксиальной серии с помощью желтой маркерной линии, С – проекция краниотомии, рассчитанная при навигации по аксиальной серии не соответствует необходимой, D – проекция каверномы на коре (стрелка) не соответствует точке выхода маркерной линии, удаление в лучшем случае будет происходить по краю краниотомии, велика вероятность что доступ придется расширять несмотря на использование навигации.
Наиболее правильный способ навигации в ране основан на поиске анатомических ориентиров. В случае конвекситальной коры удобным является использование индивидуального рисунка борозд и извилин [18]. Для сегментации головного мозга наиболее быстро и качественно нам удавалось по 3D T1 последовательности без контраста (3D T1 FSPGR BRAVO) с помощью сегментации методом водораздела (см. видео). Подчеркнем что для сегментации коры снимки должны быть без контраста, поскольку оболочки после контрастирования становятся изоинтенсивными и сливаются с мозговым веществом. Для последующей сегментации поверхностных сосудов можно использовать постконтрастные снимки.
При разметке доступа без использования нейронавигатора прибегают к использованию стандартных скелетотопических и наружных ориентиров, например ушной раковины, бровей, кожных неровностей [19]. В этом случае точность, достаточная для планирования малой краниотомии, возможна только при расположении образования в непосредственной близости от одного из ориентиров, а в случае мягкотканной структуры точность снижается с увеличенем подвижности кожи. Чтобы обнажить заданную область без нейронавигации краниотомии в лобной и теменных областях как правило делают достаточно большими (от 5 сантиметров), при этом часто искомое образование приходится удалять «по краю распила».
Для обеспечения максимально точной разметки места разреза нами разработана методика создания индивидуальных 3д печатных краниометрических линеек, использующих для позиционирования как опорные точки-неровности, так и индивидуальную кривизну головы пациента. Нами создан полуавтоматизированный алгоритм, позволяющий создавать подобные модели в течении 3-7 минут с последующей печатью в течение 2-4 часов. Мы предпочитали печать PET-g, так как этот пластик менее требователен к обдуву, что позволяет печатать быстрее. Отметим что как время моделирования, так и время печати не является «временем операции». Помогает так же возможность запуска заданий на печать удаленно. После завершения требуется отделить от модели поддержки не повредив ее, для чего надо иметь некоторый навык, однако в ряде случаев поддержки можно и не отделять.
Описанный способ подготовки и печати индивидуальных краниометрических линеек отличается низкой ценой при использовании пластика даже высокого качества. FDM принтеры имеют большой ресурс, могут функционировать без какого-либо сервиса годами, ремонтопригодны.
Заключение
Предложенный нами способ навигации для удаления конвекситальных образований головного мозга показал себя удобным и эффективным. Мы считаем что рассмотреть использование данного способа ориентирования следует даже клиникам, рутинно использующим нейронавигацию в операционной. Использование шаблонов в нейрохирургии на текущий момент представлено очень ограничено, однако имеет значительный потенциал. Например можно использовать шаблоны для выполнения доступов с сохранением воздухоносных пазух при из сложной контурной анатомии. Так же можно выполнять запланированные резекции, например, гиперостотических образований с последующей установкой предсозданного импланта.
Ссылка на оригинальную статью
https://doi.org/10.1016/j.stlm.2022.100079
Видео с вариантом процесса моделирования краниометрической линейки
Список литературы
1. Enchev Y. Neuronavigation: geneology, reality, and prospects. Neurosurg Focus. 2009 Sep;27(3):E11. doi: 10.3171/2009.6.FOCUS09109. PMID: 19722813.
2. Wang MN, Song ZJ. Classification and analysis of the errors in neuronavigation. Neurosurgery. 2011 Apr;68(4):1131-43; discussion 1143. doi: 10.1227/NEU.0b013e318209cc45. PMID: 21242841.
3. Matula C, Rössler K, Reddy M, Schindler E, Koos WT. Intraoperative computed tomography guided neuronavigation: concepts, efficiency, and work flow. Comput Aided Surg. 1998;3(4):174-82. doi: 10.1002/(SICI)1097-0150(1998)3:43.0.CO;2-G. PMID: 10027491.
4. Randazzo M, Pisapia JM, Singh N, Thawani JP. 3D printing in neurosurgery: A systematic review. Surg Neurol Int. 2016 Nov 14;7(Suppl 33):S801-S809. doi: 10.4103/2152-7806.194059. PMID: 27920940; PMCID: PMC5122816.
5. Tian Y, Chen C, Xu X, Wang J, Hou X, Li K, Lu X, Shi H, Lee ES, Jiang HB. A Review of 3D Printing in Dentistry: Technologies, Affecting Factors, and Applications. Scanning. 2021 Jul 17;2021:9950131. doi: 10.1155/2021/9950131. PMID: 34367410; PMCID: PMC8313360.
6. Mora MA, Chenin DL, Arce RM. Software tools and surgical guides in dental-implant-guided surgery. Dent Clin North Am. 2014 Jul;58(3):597-626. doi: 10.1016/j.cden.2014.04.001. PMID: 24993925.
7. Liang B, Chen Q, Liu S, Chen S, Yao Q, Wei B, Xu Y, Tang C, Wang L. A feasibility study of individual 3D-printed navigation template for the deep external fixator pin position on the iliac crest. BMC Musculoskelet Disord. 2020 Jul 21;21(1):478. doi: 10.1186/s12891-020-03509-6. PMID: 32693799; PMCID: PMC7372844.
8. Hu X, Zhong M, Lou Y, Xu P, Jiang B, Mao F, Chen D, Zheng P. Clinical application of individualized 3D-printed navigation template to children with cubitus varus deformity. J Orthop Surg Res. 2020 Mar 19;15(1):111. doi: 10.1186/s13018-020-01615-8. PMID: 32192482; PMCID: PMC7081535.
9. Liang W, Han B, Hai JJ, Hai Y, Chen L, Kang N, Yin P. 3D-printed drill guide template, a promising tool to improve pedicle screw placement accuracy in spinal deformity surgery: A systematic review and meta-analysis. Eur Spine J. 2021 May;30(5):1173-1183. doi: 10.1007/s00586-021-06739-x. Epub 2021 Feb 8. PMID: 33558972.
10. Pijpker PAJ, Kraeima J, Witjes MJH, Oterdoom DLM, Vergeer RA, Coppes MH, Groen RJM, Kuijlen JMA. Accuracy of Patient-Specific 3D-Printed Drill Guides for Pedicle and Lateral Mass Screw Insertion: An Analysis of 76 Cervical and Thoracic Screw Trajectories. Spine (Phila Pa 1976). 2021 Feb 1;46(3):160-168. doi: 10.1097/BRS.0000000000003747. PMID: 33093310; PMCID: PMC7787187.
11. Mobbs RJ, Choy WJ, Singh T, Cassar L, Davidoff C, Harris L, Phan K, Fiechter M. Three-Dimensional Planning and Patient-Specific Drill Guides for Repair of Spondylolysis/L5 Pars Defect. World Neurosurg. 2019 Dec;132:75-80. doi: 10.1016/j.wneu.2019.08.112. Epub 2019 Aug 27. PMID: 31470159.
12. Li Y, Cheng H, Li Z, Zhao H, Wang J, Wang P, Jin T, Zheng G, Ye H, Li S, Zhang J. Clinical Value of 3D-Printed Navigation Technology Combined with Neuroendoscopy for Intracerebral Hemorrhage. Transl Stroke Res. 2021 Dec;12(6):1035-1044. doi: 10.1007/s12975-021-00893-6. Epub 2021 Jan 25. PMID: 33492652.
13. Wang Q, Guo W, Liu Y, Shao W, Li M, Li Z, Li C, Li Z. Application of a 3D-Printed Navigation Mold in Puncture Drainage for Brainstem Hemorrhage. J Surg Res. 2020 Jan;245:99-106. doi: 10.1016/j.jss.2019.07.026. Epub 2019 Aug 12. PMID: 31415935.
14. Okishev DN, Podoprigora AE, Belousova OB, Pilipenko YV, Shechtman OD, Lasunin NV, Belyaev AY, Poshataev VK, Kutin MA, Konovalov AN, Spiru AM, Okisheva EA, Eliava SS. Individual'noe predoperatsionnoe 3D-modelirovanie sosudistoĭ patologii golovnogo mozga [Individual preoperative 3D modeling of vascular brain pathology]. Zh Vopr Neirokhir Im N N Burdenko. 2019;83(4):34-45. Russian. doi: 10.17116/neiro20198304134. PMID: 31577268.
15. Gerard IJ, Kersten-Oertel M, Hall JA, Sirhan D, Collins DL. Brain Shift in Neuronavigation of Brain Tumors: An Updated Review of Intra-Operative Ultrasound Applications. Front Oncol. 2021 Feb 8;10:618837. doi: 10.3389/fonc.2020.618837. PMID: 33628733; PMCID: PMC7897668.
16. Gerard IJ, Kersten-Oertel M, Petrecca K, Sirhan D, Hall JA, Collins DL. Brain shift in neuronavigation of brain tumors: A review. Med Image Anal. 2017 Jan;35:403-420. doi: 10.1016/j.media.2016.08.007. Epub 2016 Aug 24. PMID: 27585837.
17. Spetzger U, Hubbe U, Struffert T, Reinges MH, Krings T, Krombach GA, Zentner J, Gilsbach JM, Stiehl HS. Error analysis in cranial neuronavigation. Minim Invasive Neurosurg. 2002 Mar;45(1):6-10. doi: 10.1055/s-2002-23583. PMID: 11932817.
18. Dale AM, Fischl B, Sereno MI. Cortical surface-based analysis. I. Segmentation and surface reconstruction. Neuroimage. 1999 Feb;9(2):179-94. doi: 10.1006/nimg.1998.0395. PMID: 9931268.
19. Stadie AT, Kockro RA, Serra L, Fischer G, Schwandt E, Grunert P, Reisch R. Neurosurgical craniotomy localization using a virtual reality planning system versus intraoperative image-guided navigation. Int J Comput Assist Radiol Surg. 2011 Sep;6(5):565-72. doi: 10.1007/s11548-010-0529-1. Epub 2010 Sep 1. PMID: 20809398. 75–80, 2019
Еще больше интересных статей
Клапанный регулятор обдува.
Подпишитесь на автора
Подпишитесь на автора, если вам нравятся его публикации. Тогда вы будете получать уведомления о его новых статьях.
Отписаться от уведомлений вы всегда сможете в профиле автора.
Модификация стойки Kromax Office 8.
Подпишитесь на автора
Подпишитесь на автора, если вам нравятся его публикации. Тогда вы будете получать уведомления о его новых статьях.
Отписаться от уведомлений вы всегда сможете в профиле автора.
Спасение котика с помощью 3D-печати
Подпишитесь на автора
Подпишитесь на автора, если вам нравятся его публикации. Тогда вы будете получать уведомления о его новых статьях.
Отписаться от уведомлений вы всегда сможете в профиле автора.












Комментарии и вопросы
Убедительно.
Разъяснение понятное. Принимае...
6 лет, PLA.
Установил Orca-слайсер:нет изо...
У меня аникубик кобра 2 про он...
У меня кобра Макс, слайсер кур...
После печати заметили что феп...