3D-печатные раковые ткани в качестве моделей для онкологических исследований
3D-печать позволяет исследователям создавать модели раковых тканей, аккуратно воспроизводящих злокачественные опухоли человеческого организма.

Успех медицинских исследования напрямую зависит от качества используемых моделей, будь то опытные животные или реплики тканей и органов in vitro. Научная лаборатория при Университете Дрекселя, специализирующаяся на биопроизводстве, использовала 3D-печать для создания моделей раковых тканей, более точно воспроизводящих реальные злокачественные опухоли, чем традиционные двухмерные тканевые культуры. Подобного рода наглядные пособия могут помочь прийти к лучшему пониманию нюансов роста опухолей и, что особенно важно, созданию методов борьбы с раковыми образованиями.
Настоящие раковые опухоли отличаются от своих искусственных лабораторных аналогов площадью, формой клеток и клеточной структурой. При испытаниях потенциальных препаратов на подобных суррогатах, искусственные клетки демонстрируют повышенную уязвимость, что ведет к завышенным оценкам эффективности.
Исследования доктора Вей Суна и его команды начались с анализа методик струйно-капельной печати клеток HeLa (известной линии «бессмертных» клеток, служащих возбудителями рака шейки матки) и структурного матрикса, аналогичного протеинам, окружающим раковые клетки в живом организме. Затем команда провела сравнительный анализ новых образцов с привычными двухмерными образцами на предмет устойчивости к химиотерапевтическим препаратам.
Особенности работы 3D-печатных устройств, а именно повышенная температура и механическое воздействие на материалы, оказывают негативное влияние на живые клетки, поэтому для начальных экспериментов использовались наиболее стойкие культуры.
В то же время, тепло необходимо для достижения соответствующей вязкости комбинации фибрина, альгината и желатина, используемой для имитации поддерживающих протеинов, в чьей среде растут живые клетки. Если температура слишком высока, раковые клетки погибают. Если слишком низка – требуется слишком сильное механическое воздействие для экструзии желатиновой смеси, что опять-таки приводит к гибели клеток. Успешная печать потребовала определения правильного баланса рабочих параметров опытным путем.
3D-печать клеток позволяет исследователям имитировать естественный рост тканей. Каналы в напечатанной структуре обеспечивают обмен воздуха, питательных веществ и отходов, как в настоящих тканях. После восьми дней наращивания, 90 процентов клеток остались живы, а ткань преобразовалась в плотную шарообразную клеточную структуру, радикально отличающуюся от двухмерных культур с плоскими, удлиненными клетками. Кроме того, деление клеток происходило повышенными темпами, как и в случае естественных раковых образований.
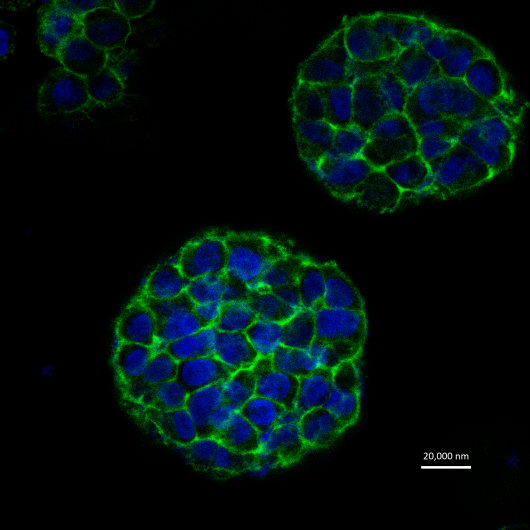
После отработки процесса печати живых тканей последовал еще более важный этап: исследователям предстояло доказать, что новые образцы являются более подходящими моделями для тестирования онкологических препаратов. Обработка химиотерапевтическим препаратом паклитакселем показала повышенное сопротивление новых культур по сравнению с привычными двухмерными образцами, сопоставимое с поведением опухолей, образующихся естественным путем.
Планы на будущее включают печать с одновременным использованием клеток разных типов для более точной имитации раковых тканей, а также нанесение напечатанных раковых клеток на здоровые напечатанные ткани для симуляции роста опухолей с целью лучшего понимания процесса.
Сун создал свой 3D-принтер в 2002 году, дабы обеспечить своей лаборатории возможность биопроизводства тканей и костных структур. Подобные устройства используются и другими исследователями с не менее впечатляющими результатами. В последнее время были созданы такие объекты, как черепа и ушные раковины из хрящевых клеток.
Предлагаем вашему вниманию видео, демонстрирующее работу 3D-биопринтера:
Статья подготовлена для 3DToday.ru
Еще больше интересных статей
Купили 3D-принтер, решили заработать. Что дальше?
Подпишитесь на автора
Подпишитесь на автора, если вам нравятся его публикации. Тогда вы будете получать уведомления о его новых статьях.
Отписаться от уведомлений вы всегда сможете в профиле автора.
Русский инженер собрал стереолитографический 3D-принтер из оптических приводов стоимостью 10000 рублей
Подпишитесь на автора
Подпишитесь на автора, если вам нравятся его публикации. Тогда вы будете получать уведомления о его новых статьях.
Отписаться от уведомлений вы всегда сможете в профиле автора.
Подробнее о 3D-печати домов – эксклюзивное интервью 3D Today c Андреем Руденко
Подпишитесь на автора
Подпишитесь на автора, если вам нравятся его публикации. Тогда вы будете получать уведомления о его новых статьях.
Отписаться от уведомлений вы всегда сможете в профиле автора.




Комментарии и вопросы
habr. com/ru/companies/madrobo...
А теперь просто прикиньте что....
Типичный вопль особенно если ч...
Возможно экструдер сносит дета...
Anet a8 после прошивки нагрев...
шестерня выглядит вот так, не...
на месте швов стали появляться...